INQUINANTE O3 - OZONO
INQUINANTE O3 - OZONO |
1) CARATTERISTICHE DELL'INQUINANTE
L'ozono è costituito da una molecola triatomica,
in equilibrio caratteristico con l'ossigeno atmosferico: O3
<=> O2 + O.
Si forma nell'aria in presenza di scariche elettriche, durante i temporali, per
azione di raggi UV, nel ciclo di fotodissociazione di NO2 e in presenza di
idrocarburi e radicali OH, quindi è un inquinante secondario conseguenza delle attività
umane e in particolare del traffico veicolare. E' dannoso per l'uomo e per l'ambiente in
quanto è un forte ossidante gassoso : entra nei processi di formazione dello smog
fotochimico e delle piogge acide. Si può formare anche a distanza da fonti di NO e HC, e
in particolare sottovento (caratteristico dei periodi estivi).
E` abbastanza curioso
che, a livello della terra, l'ozono sia considerato dannoso: in effetti è uno dei
maggiori componenti fotochimici dello smog. Invece, se non fosse presente nella
stratosfera noi non potremmo sopravvivere: lassù assorbe molti raggi ultravioletti
potenzialmente dannosi (alle lunghezze d'onda tra 240 e 320 nm) che possono causare tumori
alla pelle e danni alla vegetazione.
L'ozono come inquinante troposferico ha aspetti caratteristici: mantiene abbastanza
costante la sua concentrazione per vaste aree, la sua formazione è ad intervalli di tempo
che variano da ore a giorni, raramente variazioni di HC e NOx (suoi precursori)
producono variazioni percentuali di concentrazione di O3 , e in certe
condizioni la loro diminuzione può produrre un aumento di O3 , inoltre
le concentrazioni sono in genere più basse vicino alle sorgenti. Le condizioni
meteorologiche che influenzano la concentrazione di O3 sono la direzione e la
velocità del vento, la stabilità atmosferica, l'altezza e lo spessore di
rimescolamento, la temperatura e l'intensità della radiazione solare.
2) FORMAZIONE DELL'INQUINANTE
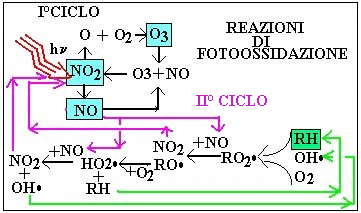 Le reazioni che
portano alla formazione dell'ozono da smog sono quelle indicate nella figura a fianco.Alle quote più basse lo smog fotochimico
è costituito da una serie di reazioni che coinvolgono il biossido di azoto: in presenza
di radiazione solare (430 nm) si scinde in O e NO; in seguito alla formazione di ozono e
alla sua combinazione con NO si riforma NO2. Questo insieme di stadi di
reazione costituisce un ciclo chiuso ( I° CICLO) poiché ogni specie
viene consumata e successivamente prodotta, e pertanto il danno è minimo.Ma il ciclo
viene aperto dalla presenza di idrocarburi e derivati (2° CICLO) e così
si avvia la formazione dei radicali fotossidanti ( fotosmog) che mostra l’accumulo di
particolari prodotti in funzione dell’ora del giorno; questa produzione particolare
è dovuta alle diverse costanti cinetiche e coefficienti di fotolisi per ogni
composto.
Le reazioni che
portano alla formazione dell'ozono da smog sono quelle indicate nella figura a fianco.Alle quote più basse lo smog fotochimico
è costituito da una serie di reazioni che coinvolgono il biossido di azoto: in presenza
di radiazione solare (430 nm) si scinde in O e NO; in seguito alla formazione di ozono e
alla sua combinazione con NO si riforma NO2. Questo insieme di stadi di
reazione costituisce un ciclo chiuso ( I° CICLO) poiché ogni specie
viene consumata e successivamente prodotta, e pertanto il danno è minimo.Ma il ciclo
viene aperto dalla presenza di idrocarburi e derivati (2° CICLO) e così
si avvia la formazione dei radicali fotossidanti ( fotosmog) che mostra l’accumulo di
particolari prodotti in funzione dell’ora del giorno; questa produzione particolare
è dovuta alle diverse costanti cinetiche e coefficienti di fotolisi per ogni
composto.
Infatti in presenza per esempio di metano avvengono reazioni formate anche da 80 stadi che
alterano l’equilibrio del ciclo.In questo caso si viene a formare un composto in
grado di ossidare l’ossido di azoto a biossido.
Questo secondo ciclo ha due effetti egualmente dannosi:
a)fa aumentare la concentrazione di biossido di azoto, molto più dannoso
dell’ossido;
b)sottrae appunto l’ossido di azoto al suo ossidante naturale, l’ozono, facendo
aumentare la concentrazione di ozono di una molecola per ogni molecola di NO che si
converte a NO2 (quindi nello schema addirittura di due).
La serie di processi sopra descritta è soltanto una piccola e semplificata parte di
quello che avviene nella formazione di un particolare fenomeno acuto di inquinamento
chiamato smog fotochimico. Altre reazioni sono possibili dato il forte potere
ossidante dell' O3, in particolare il ciclo del radicale ossidrile, che è
nocivo per l'uomo in quanto attacca le membrane cellulari:
O3 = O + O2 ;
O + H2O = 2 OH ;
OH + O3 = H2O + O2 ;
H2O + NO = OH + NO2 .
3) EFFETTI
L'ozono è tossico per gli esseri viventi, in quanto attacca la struttura
cellulare degli organismi. Per l'uomo si hanno danni alle vie respiratorie e ai polmoni,
che provocano l'insorgere di malattie acute e croniche, tosse e infiammazioni;inoltre
provoca irritazione agli occhi.
Tra gli effetti dell’inquinamento sui vegetali ci sono quelli costituiti sulle
piante da piccoli puntini necrotici di colore che va dal bianco al nero (vedere al
riguardo la parte sugli effetti dell'inquinamento sui vegetali ); a seconda della concentrazione e della durata
dell'attacco con ozono, oltre alla necrosi delle foglie si può avere diminuzione della
crescita delle piante.
Un effetto indiretto dell'ozono è che contribuisce alla formazione dei radicali OH*, che
vanno ad abbassare la concentrazione dell' NO, permettendo ai radicali perossoacetilici (
di provenienza da scarichi di idrocarburi) di formare con l' NO2 i perossiacilnitrati (PAN), tossici per l'uomo.
L'ozono è un degradante di tutti i materiali organici, materie plastiche e gomme, che
provoca invecchiamento infragilimento e scolorimento.
4) LIMITAZIONE
DELL'INQUINANTE
Considerato che la
fonte principale di O3 è il traffico veicolare, nelle giornate in cui le
condizioni meteo sono favorevoli alla sua formazione si cerca di limitare il traffico
soprattutto nelle ore mediane del giorno.
5) LIMITI DI LEGGE
Livelli di attenzione e di
allarme rispettivamente 180 e 360 mg/m3.